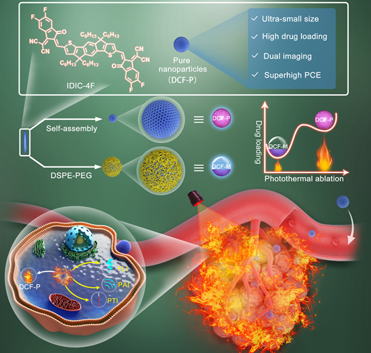
光热治疗作为一类非浸入性疗法受到越来越多关注。为了使光热转化剂具有较好水溶性,一般会采用聚乙二醇(PEG)等双亲性物质包裹光热转化剂,制备成纳米粒子再用于肿瘤的光热治疗。辅助性双亲物质的采用,一方面导致光热转化剂在纳米粒子内部排列杂乱无序,增加纳米粒子尺寸,进而影响其光热转化效率;另一方面,辅助性双亲物质在纳米粒子体内转运过程会发生脱落,对正常器官也会引发副作用。因此,发展无载体纳米粒子,是改善光热转化剂光热性能,减弱辅助性双亲物质对正常器官副作用的重要途径。
基于上述理念,纳米医学光子学实验室科研人员以共轭有机小分子 IDIC-4F为研究对象,通过自组装和纳米沉淀法,制备了仅含有IDIC-4F的超小纳米粒子DCF-P(直径约 4 nm)和IDIC /PEG纳米粒子DCF-M(直径约44 nm),两类纳米粒子在不同溶解媒介中均具有较好稳定性,为其生物医学应用提供了前提条件。DCF-P和DCF-M包载率测试显示,DCF-P纳米粒子中IDIC-4F含量约为100%,较DCF-M纳米粒子IDIC-4F含量提高了15倍(6.02%),表明自组装制备纳米粒子可大幅度提高光热转换剂含量。X-射线衍射结果表明,IDIC-4F在DCF-P纳米粒子中高度有序排列,光热性能显示,DCF-P的光热转换效率高达80.5%,较DCF-M(57.3%)提高了40%,表明分子高度有序排列可显著影响纳米粒子光热性能。随后,科研人员评价其在体外抑制肿瘤细胞增殖的性能,研究显示,660 nm激光照射下(5 W cm-2, 5 min),DCF-P对人非小细胞肺癌细胞A549和H1299均具有较好抑制增殖作用,其半数抑制浓度(IC50)约为7.88 µg mL-1(A549),较DCF-M(12.73 µg mL-1)降低了39%。进一步体内抗肿瘤性能研究表明,DCF-P可高效抑制A549皮下瘤生长,小鼠体重测试,血液生化指标评价和主要器官组织学分析均无异常,表明了DCF-P较优异的抑制肿瘤生长性能和良好生物兼容性。其分子作用机制研究揭示,DCF-P主要引发了肿瘤细胞的凋亡和坏死,进而抑制了肿瘤增殖。该研究发现了一类高包载率光热转换剂制备方法,验证了无载体包裹纳米粒子高效光热诊疗性能,证明了分子高度有序排列可显著影响其光热性能的新理念,提供了调控光热转换剂性能的新策略。相关研究结果以《Carrier-Free Delivery of Ultra-small π-Conjugated Oligomer Nanoparticles with Photothermal Conversion over 80% for Cancer Theranostics》为题目发表于国际著名期刊Small (2021, DOI: 10.1002/smll.202104521, IF = 13.3)。
上述研究工作河南大学基础医学院纳米医学光子学实验室为第一完成单位,2019级硕士研究生郑日杰和苏州大学赵琦博士为共同第一作者,河南大学刘中华博士和黄永伟博士为通讯作者,研究工作得到国家自然科学基金、河南省杰出青年基金和河南省高校科技创新团队支持计划等项目的经费支持。